CRISPR – pengulangan palindromik pendek yang dikelompokkan secara teratur dan diselingi – adalah jawaban dunia mikroba terhadap kekebalan adaptif. Bakteri tidak menghasilkan antibodi ketika mereka diserang oleh patogen dan kemudian memblokir antibodi tersebut jika mereka bertemu dengan patogen yang sama lagi, seperti yang kita lakukan. Sebaliknya, mereka mengintegrasikan beberapa DNA patogen ke dalam genom mereka dan menempelkannya ke enzim yang dapat mereka gunakan untuk mengenali urutan DNA patogen dan memotongnya menjadi beberapa bagian jika patogen tersebut muncul kembali.
Enzim yang melakukan pemotongan disebut Cas, diambil dari nama CRISPR. Meskipun sistem CRISPR-Cas berevolusi sebagai mekanisme pertahanan bakteri, sistem ini telah dimanfaatkan dan diadaptasi oleh para peneliti sebagai alat yang ampuh untuk manipulasi genetik dalam penelitian laboratorium. Obat ini juga telah terbukti penggunaannya dalam bidang pertanian, dan pengobatan berbasis CRISPR pertama telah disetujui di Inggris untuk mengobati penyakit sel sabit dan talasemia beta yang bergantung pada transfusi.
Kini, para peneliti telah mengembangkan cara baru untuk mencari genom untuk sistem mirip CRISPR-Cas. Mereka menemukan bahwa kami mungkin memiliki banyak alat tambahan untuk digunakan.
Modifikasi DNA
Hingga saat ini, enam jenis sistem CRISPR-Cas telah diidentifikasi pada mikroba yang berbeda. Meskipun detailnya berbeda, semuanya memiliki daya tarik yang sama: mereka mengirimkan protein ke rangkaian materi genetik tertentu dengan tingkat kekhususan yang hingga kini secara teknis sulit, mahal, dan memakan waktu untuk dicapai. Urutan DNA apa pun yang menarik dalam sistem dapat diprogram dan ditargetkan.
Sistem asli pada mikroba biasanya membawa eksonuklease – enzim yang membelah DNA – ke dalam rangkaiannya, memotong materi genetik patogen. Kemampuan ini dapat digunakan untuk memotong urutan DNA yang dipilih untuk pengeditan gen; Dikombinasikan dengan enzim dan/atau rangkaian DNA lainnya, ini dapat digunakan untuk menyisipkan atau menghapus rangkaian pendek tambahan, dan untuk mengoreksi gen mutan. Beberapa sistem CRISPR-Cas memotong molekul RNA tertentu, bukan DNA. Mereka dapat digunakan untuk menghilangkan RNA penyebab penyakit, seperti genom beberapa virus, dengan cara menghilangkannya pada bakteri asli. Ini juga dapat digunakan untuk menyelamatkan cacat dalam pemrosesan RNA.
Namun ada banyak cara tambahan untuk memodifikasi asam nukleat yang mungkin berguna. Masih menjadi pertanyaan apakah enzim yang melakukan modifikasi tambahan telah berevolusi. Jadi beberapa peneliti memutuskan untuk mencarinya.
Para peneliti di MIT telah mengembangkan alat baru untuk mendeteksi varian susunan CRISPR dan menerapkannya pada 8,8 tera (1.012) pasangan basa informasi genom prokariotik. Banyak dari sistem yang mereka temukan bersifat langka dan hanya muncul dalam kumpulan data dalam 10 tahun terakhir. Hal ini menyoroti betapa pentingnya untuk terus menambahkan sampel lingkungan yang sebelumnya sulit diperoleh ke dalam repositori data ini.
Alat baru ini diperlukan karena basis data rangkaian protein dan asam nukleat berkembang dengan kecepatan yang sangat tinggi, sehingga teknik untuk menganalisis semua data tersebut perlu terus diperbarui. Beberapa algoritme yang digunakan untuk menganalisisnya mencoba membandingkan setiap rangkaian dengan rangkaian lainnya, yang jelas tidak dapat dipertahankan jika menangani miliaran gen. Yang lain mengandalkan pengelompokan, tetapi hanya menemukan gen yang sangat mirip, sehingga tidak dapat menjelaskan hubungan evolusi antara protein yang berkerabat jauh. Namun pengelompokan berbasis hashtag yang cepat dan peka lokasi (“perakitan flash”) bekerja dengan mengelompokkan miliaran protein ke dalam kumpulan rangkaian yang lebih kecil dan lebih besar yang hanya berbeda sedikit untuk mengidentifikasi kerabat baru dan langka.
Pencarian menggunakan FLSHclust berhasil mengekstraksi 188 sistem CRISPR-Cas baru.
Banyak Renyahnya
Beberapa tema muncul dari karya tersebut. Salah satunya adalah beberapa sistem CRISPR yang baru diidentifikasi menggunakan enzim Cas dengan domain yang belum pernah terlihat sebelumnya, atau tampak seperti fusi dengan gen yang diketahui. Para ilmuwan juga mengkarakterisasi beberapa enzim ini dan menemukan bahwa salah satu enzim ini lebih spesifik daripada enzim CRISPR yang saat ini digunakan, dan enzim lain yang memotong RNA yang mereka usulkan memiliki struktur yang cukup berbeda untuk memasukkan sistem CRISPR-Cas tipe 7 yang sepenuhnya baru.
Akibat wajar dari topik ini adalah menghubungkan enzim dengan fungsi berbeda, tidak hanya nuklease (enzim yang memotong DNA dan RNA), dengan susunan CRISPR. Para ilmuwan telah mengeksploitasi kemampuan luar biasa CRISPR untuk menargetkan gen dengan menempelkannya pada jenis enzim dan molekul lain, seperti pewarna fluoresen. Namun ternyata evolusi sampai di sana terlebih dahulu.
Misalnya, FLSHclust mengidentifikasi sesuatu yang disebut transposase yang dikaitkan dengan dua jenis sistem CRISPR yang berbeda. Transposase adalah enzim yang membantu mentransfer bagian tertentu dari DNA ke bagian lain dari genom. Transformasi yang diarahkan oleh CRISPR RNA telah terlihat sebelumnya, tetapi ini adalah contoh lainnya. Berbagai macam protein dengan fungsi berbeda, seperti protein dengan domain transmembran dan molekul pemberi sinyal, telah ditemukan terkait dengan susunan CRISPR, menyoroti sifat padu padan dari evolusi sistem ini. Mereka bahkan menemukan protein yang diekspresikan oleh virus yang mengikat rangkaian CRISPR dan menjadikannya tidak aktif, dan virus tersebut pada dasarnya menonaktifkan sistem CRISPR yang berevolusi untuk melindungi dari virus.
Para peneliti tidak hanya menemukan protein baru yang terkait dengan susunan CRISPR, mereka juga menemukan susunan berulang yang berjarak teratur dan tidak terkait dengan enzim Cas, mirip dengan CRISPR tetapi tidak dengan CRISPR. Mereka tidak yakin dengan fungsi sistem yang dipandu RNA ini tetapi berspekulasi bahwa mereka terlibat dalam pertahanan seperti halnya CRISPR.
Para penulis berangkat untuk menemukan “daftar protein yang dipandu RNA yang memperluas pemahaman kita tentang biologi dan evolusi sistem ini dan memberikan titik awal untuk pengembangan bioteknologi baru.” Dan mereka tampaknya telah mencapai tujuan mereka: “Hasil dari pekerjaan ini mengungkapkan fleksibilitas regulasi dan fungsional serta modularitas sistem CRISPR yang belum pernah terjadi sebelumnya,” tulis mereka. Mereka kemudian menyimpulkan: “Ini hanya mewakili sebagian kecil dari sistem yang ditemukan, namun hal ini menyoroti betapa luasnya potensi keanekaragaman hayati bumi yang belum dimanfaatkan.” Kandidat yang tersisa akan menjadi sumber daya untuk eksplorasi di masa depan.
Artikel DOI: 10.1126/sains.adi1910






More Stories
Legiuner berangkat dalam dua kapal pesiar terpisah yang terkait dengan fitur kemewahan khusus ini: lapor
Setelah 120 tahun tumbuh, bambu Jepang baru saja berbunga, dan itu menjadi masalah
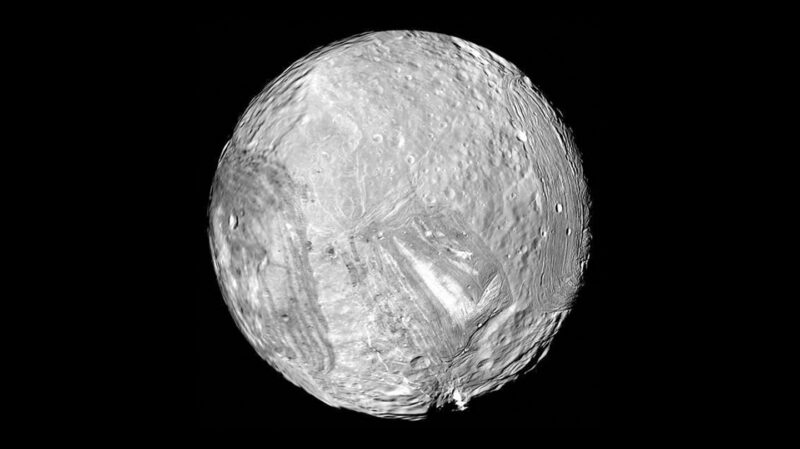
Bukti adanya lautan di bulan Uranus, Miranda, sungguh mengejutkan