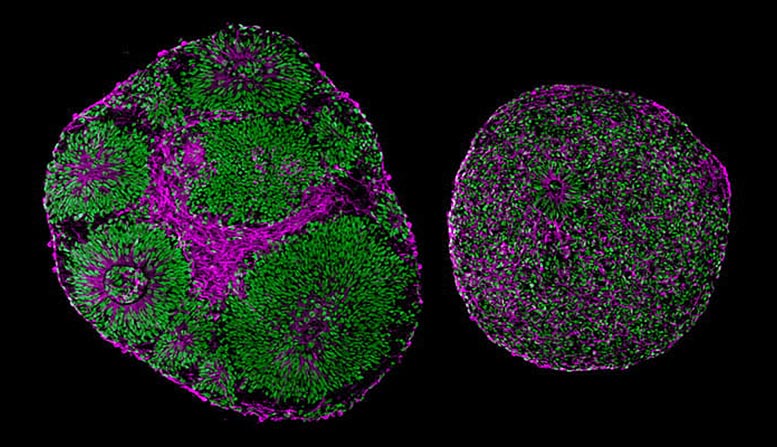
Mikrograf mengungkapkan perbedaan yang signifikan dalam ukuran dan struktur antara organel otak yang berasal dari pasien dengan sindrom Pitts Hopkins (kanan) dan kontrol (kiri). Kredit: Universitas California, Ilmu Kesehatan San Diego
Studi University of California San Diego (UCSD) menggunakan jaringan otak manusia yang dikembangkan di laboratorium untuk mengidentifikasi kelainan neurologis pada sindrom Pitt Hopkins dan menguji alat terapi gen.
Dalam sebuah penelitian yang diterbitkan pada 2 Mei 2022 di jurnal Komunikasi AlamPara ilmuwan di University of California, San Diego School of Medicine, menggunakan organoid otak manusia untuk menemukan bagaimana mutasi genetik yang terkait dengan autisme parah mengganggu perkembangan saraf. Penggunaan alat terapi gen untuk mengembalikan fungsi gen telah berhasil menyelamatkan struktur dan fungsi saraf.
Beberapa penyakit neurologis dan neuropsikiatri, termasuk gangguan spektrum autisme (ASD) dan skizofrenia, telah dikaitkan dengan mutasi pada faktor transkripsi 4 (TCF4), sebuah gen yang penting dalam perkembangan otak. Faktor transkripsi mengatur kapan gen lain dihidupkan atau dimatikan, sehingga ada atau tidak adanya mereka, dapat memiliki efek domino pada janin yang sedang berkembang. Namun, tidak banyak yang diketahui tentang apa yang terjadi pada otak manusia ketika ini terjadi TCF4 bermutasi.
Untuk mengeksplorasi pertanyaan ini, para peneliti berfokus pada sindrom Pitts Hopkins, gangguan spektrum autisme yang disebabkan oleh mutasi pada TCF4. Anak-anak dengan kondisi keturunan memiliki cacat kognitif dan motorik yang mendalam dan biasanya nonverbal.
Sindrom Pitt Hopkins (PTHS) adalah kelainan genetik langka yang ditandai dengan keterlambatan perkembangan, epilepsi, fitur wajah yang khas, dan hiperventilasi yang berpotensi intermiten diikuti oleh apnea. Seperti lebih banyak ditemukan tentang Pitt Hopkins, spektrum perkembangan gangguan meluas untuk memasukkan autisme, kecemasan, ADHD, dan gangguan sensorik. Ini terkait dengan cacat dalam kromosom 18, khususnya ekspresi gen TCF4 yang tidak mencukupi.
Model tikus yang ada sindrom Pitt Hopkins gagal untuk secara akurat meniru karakteristik neurologis pasien, sehingga tim UCSF menciptakan model penelitian manusia untuk gangguan tersebut. Menggunakan teknologi sel punca, mereka mengubah sel kulit pasien menjadi sel punca, yang kemudian dikembangkan menjadi organel otak tiga dimensi, atau “otak mini”.
Pengamatan awal organoid otak mengungkapkan sejumlah besar perbedaan struktural dan fungsional antara TCF4Sampel mutagen dan kontrolnya.
Penulis senior studi Alison R. Mottery, Ph.D., profesor di UCSD School of Medicine, direktur Program Sel Induk UCSD, dan anggota Sanford Consortium for Regenerative Medicine mengatakan.
Itu TCF4Organel mutan jauh lebih kecil dari organel normal, dan banyak sel sebenarnya bukan neuron, tetapi nenek moyang neuron. Sel-sel sederhana ini seharusnya berkembang biak dan kemudian matang menjadi sel-sel otak khusus, tetapi pada organel yang bermutasi, bagian dari proses ini menjadi serba salah.
Serangkaian eksperimen mengungkapkan bahwa TCF4 Ledakan menyebabkan gangguan pada aliran sungai SOX Gen dan jalur Wnt, dua sinyal molekuler penting yang memandu sel embrio untuk berkembang biak, matang menjadi neuron, dan pindah ke tempat yang benar di otak.
Karena ketidakseimbangan regulasi ini, neurit tidak berproliferasi secara efisien dan oleh karena itu lebih sedikit neuron kortikal yang diproduksi. Sel-sel yang telah matang menjadi neuron kurang bersemangat dari biasanya dan sering terus berkerumun bersama daripada mengatur diri mereka sendiri ke dalam sirkuit saraf yang disetel dengan baik.
Struktur seluler atipikal ini mengganggu aliran aktivitas saraf di organel otak yang bermutasi, yang menurut penulis kemungkinan akan berkontribusi pada gangguan fungsi kognitif dan motorik.
“Kami terkejut melihat masalah pembangunan besar di semua tingkat yang berbeda ini, dan itu membuat kami bertanya-tanya apa yang dapat kami lakukan untuk mengatasinya,” kata penulis pertama Fabio Papez, PhD, profesor di University of Campinas dan peneliti tamu di UCLA . Fakultas Kedokteran San Diego, yang bersama-sama mengawasi pekerjaan dengan Muotri. Papes memiliki kerabat yang menderita sindrom Pitts Hopkins, yang mendorongnya untuk belajar TCF4.
Tim menguji dua strategi terapi gen yang berbeda untuk mengembalikan gen fungsional di jaringan otak. Kedua metode secara efektif meningkat TCF4 Dengan demikian, fenotipe sindrom Pitt Hopkins dikoreksi pada tingkat molekuler, seluler, dan elektrofisiologis.
“Fakta bahwa kita dapat memperbaiki gen ini dan bahwa seluruh sistem saraf membangun kembali dirinya sendiri, bahkan pada tingkat fungsional, sungguh menakjubkan,” kata Mootri.
Mootri mencatat bahwa intervensi genetik ini terjadi pada tahap pranatal perkembangan otak, sementara dalam pengaturan klinis, anak-anak akan menerima diagnosis dan pengobatan mereka beberapa tahun kemudian. Dengan demikian, uji klinis harus terlebih dahulu mengkonfirmasi apakah intervensi selanjutnya masih aman dan efektif. Tim saat ini sedang menyempurnakan alat terapi gen berlisensi baru-baru ini sebagai persiapan untuk uji coba semacam itu, di mana diharapkan injeksi tulang punggung vektor gen akan mengembalikan fungsi TCF4 di otak.
“Untuk anak-anak ini dan orang yang mereka cintai, setiap peningkatan fungsi kognitif-motorik dan kualitas hidup patut dicoba,” kata Mootri.
“Hal yang sangat istimewa tentang pekerjaan ini adalah bahwa para peneliti ini melampaui lab dan bekerja sangat keras untuk membuat temuan ini dapat diterjemahkan ke klinik,” kata Audrey Davido, presiden Pitt Hopkins Foundation for Research. “Ini lebih dari sekadar makalah akademis yang luar biasa; ini adalah ukuran sebenarnya dari apa yang dapat dicapai oleh sains yang berpengalaman dengan harapan dapat mengubah kehidupan manusia menjadi lebih baik.”
Referensi: “Hilangnya faktor transkripsi 4 dikaitkan dengan defisit dalam proliferasi progenitor dan konten neuron kortikal” oleh Fabio Papis, Antonio B. Camargo, Janina S. De Souza, Vinicius MA, Carvalho, Ryan A. Seto, Irene Lamontani, Jose R. Teixeira, Simone H. Avancini, Sandra M. Sanchez Sanchez, Thiago S. Nakahara, Carolina N. Santo, Wei Wu, Hang Yao, Barbara M. P. Araujo, Paolo Enf Filho, dan Gabriel J. , 2 Mei 2022, Komunikasi Alam.
DOI: 10.1038 / s41467-022-29942-w
Rekan penulis adalah: Janina S. de Souza, Ryan A. Sito, Irene Lamontani, Simone H. Avancini, Sandra M. Sanchez Sanchez, Wei Wu, Hang Yao, dan Gabriel Haddad di UCSD; Antonio B. Camargo, Vinicius MA Carvalho, Jose R Teixeira, Thiago S. Nakahara, Carolina N Santo, Barbara MB Araujo dan Paulo Enf Filho di Universitas Campinas.
Pekerjaan ini didanai sebagian oleh National Institutes of Health (hibah R01 MH123828), Yayasan Penelitian Pitts Hopkins, Yayasan Penelitian São Paulo (hibah 2020/11451-7, 2018/03613-7, 2018/04240-0) dan Institut Genom Gabungan Kementerian Kesehatan Energi Amerika (DE-AC02-05CH11231).
Pengungkapan: Alison R. Mootri adalah salah satu pendiri TISMOO, sebuah perusahaan yang didedikasikan untuk analisis genetik dan organogenesis otak manusia dan memiliki kepentingan ekuitas.

“Kutu buku musik lepas. Pecandu internet bersertifikat. Pencinta perjalanan. Penyelenggara hardcore. “








More Stories
Makanan dan minuman yang menyebabkan nyeri sendi menurut dokter
Komet Pons-Brooks: Bagaimana dan kapan melihatnya
Sebuah lubang hitam besar telah terlihat kurang dari 2.000 tahun cahaya dari Bumi